


Chronologie relative et échelle des temps

Cours
Chronologie relative : principes

Cours
L'échelle stratigraphique
La chronologie absolue

Cours
Chronologie absolue: principes

Cours
La datation au Carbone 14

Cours
La datation au Potassium Argon

Cours
La datation au Rubidium/Strontium
Exercices

Exercice
Vocabulaire
La datation au Carbone 14
Sommaire
Choix des éléments à dater
Propriété
Le carbone 14 est un élément dont le noyau est constitué de 6 protons et de 8 neutrons. Le carbone 14 se forme à partir d’un azote 14 bombardé par un neutron provenant des particules brisées par les rayons cosmiques au niveau de l’atmosphère.
Il se retrouve dans les molécules de dioxyde de carbone. Il va donc être intégré à la matière organique végétale lors de la photosynthèse puis à la matière organique animale par la chaîne alimentaire. Cette méthode est donc utilisée pour dater des restes d’êtres vivants.
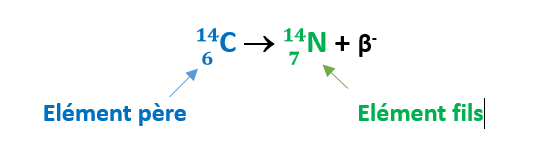
Le carbone 14 est caractérisé par la présence de 2 neutrons excédentaires. Le retour à l’état stable se fait par émission β- (émission d’un électron).
Cet isotope a une période radioactive relativement courte à l’échelle des temps géologiques. Sa demi-vie est de T = 5730 ans.
Ainsi en appliquant la formule:
Le carbone 14 permet donc de dater des périodes qui n’excèdent pas 50 000 ans au maximum (10x la période ou demi-vie).
Méthode
À la fermeture du système, c'est-à-dire à la mort de l’organisme, le 14C n’est plus intégré à la matière et sa quantité Po va commencer à diminuer en raison des désintégrations.
Le ratio atmosphérique et donc organique, est de :
La constante de désintégration du carbone 14 est :
Ce qui équivaut à 13.56 désintégrations par minute et par gramme de carbone.
Ce ratio est stable dans le temps. C’est pourquoi, on admet qu’au moment de la fermeture du système, la proportion de 14C était la même que pour un organisme actuel car selon le principe d’actualisme, on considère qu’un individu incorpore la même quantité de carbone 14 quelle que soit l’époque. Cette proportion de 14C initial est donc connue.
Il existe 2 moyens de calculer l’âge d’un échantillon :
Soit en mesurant la proportion de 14C dans l’échantillon à dater.
Soit en mesurant la radioactivité de l’échantillon.
Calcul de l’âge en utilisant la proportion de 14C mesurée dans l’échantillon à dater
Le spectromètre de masse mesure la proportion de 14C dans l’échantillon à dater.
Il mesure donc le rapport
ce qui équivaut à dire :
Car le taux de 12C est constant.
Le rapport « ro » est le rapport initial
On transforme alors la formule :
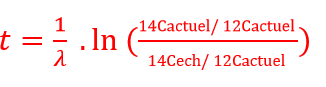
Calcul de l’âge en utilisant la radioactivité de l’échantillon à dater
Il est possible d’utiliser une autre mesure que celle du spectromètre de masse.
Le Becquerel (Bq) mesure l’activité de la source radioactive, c’est-à-dire le nombre de noyaux qui se transforment et émettent un rayonnement par seconde.
On exprime l’activité d’un objet, d’un aliment,… en Becquerel par kilo, par litre,… Sachant que l’activité radioactive actuelle du 14C est de 1.130 Bq et qu’elle était la même au moment de la fermeture du système, il suffit donc de mesurer à l’aide d’un compteur geiger, l’activité radioactive de l’élément à dater pour retrouver son âge.
On a:
On simplifie la fraction et on obtient:
Exemple 1
Un tronc fossilisé présente une radioactivité de 8.56 désintégrations par minute et par gramme. La radioactivité naturelle du bois est de 13.56 désintégrations par minute et par gramme.
Consigne : Retrouvez l’âge du tronc d’arbre fossilisé.
On utilise ici les mesures de radioactivité. On utilise donc la formule :
On sait que :
On obtient:
Exemple 2
Lors d’explosions volcaniques récentes en Auvergne, des forêts ont été enfouies sous les cendres. On peut aujourd’hui dater ces éruptions en déterminant le quotient du nombre d’atomes de carbone 14 par le nombre d’atomes de carbone 12 dans les bois fossilisés :
Lieu du gisement en Auvergne | Quotient |
Montcyneire | |
Lassolas |
Consigne : Retrouvez l’âge des éruptions.
On travaille ici non pas avec la mesure de la radioactivité mais avec les rapports mesurés par le spectromètre.
La formule à utiliser est donc :
On a :
Il suffit de remplacer les valeurs dans la formule et on trouve :
Revenir au chapitre
Commentaires





