


Glucose et glycémie

Cours
Glucose et glycémie

Cours
La régulation de la glycémie

Cours
Les dysfonctionnements de la régulation glycémique : les diabètes
Exercices

Exercice
Vocabulaire
Les dysfonctionnements de la régulation glycémique : les diabètes
Sommaire
Introduction
Quand le système réglant est défaillant, l’homéostasie n’est plus maintenue et la glycémie varie. Quand on observe après 2 mesures à jeun, une glycémie de plus de 1.26 g.L-1, ou une glycémie supérieure à 2 g.L-1 à n’importe quel moment de la journée, on parle de diabète.
Un test d’hyperglycémie provoquée orale ou HGPO consistant à mesurer les variations de la glycémie après avoir ingéré 75g de glucose à jeun permet de confirmer le diagnostic.
Le sucre accumulé dans le sang est éliminé par le rein dans de grandes quantités d’urine (polyurie) contenant du sucre absent en temps normal (glycosurie). Cette polyurie provoque une soif intense (polydipsie). La faible assimilation de sucre par les cellules provoque une accentuation de l’appétit (polyphagie). On observe un amaigrissement malgré la prise de nourriture abondante. Cet amaigrissement touche aussi bien les myocytes que les adipocytes ce qui explique la grande faiblesse des diabétiques, faiblesse pouvant atteindre le stade de la léthargie.
On note également une acidocétose. C’est une accumulation d'acétone provenant de la forte dégradation des lipides du tissu adipeux pendant l’amaigrissement. L’acétone est à l’origine des perturbations gastriques et on observe une haleine caractéristique (odeur de pomme de reinette). L’acétone sera également retrouvée dans les urines.
On peut également noter une acidose provoquant des troubles respiratoires et neurologiques (stupeur, syndrome confusionnel voire coma). Enfin des troubles de la vision sont régulièrement observés : la vue devient brutalement floue.
Les diabétiques sont souvent plus sensibles aux infections urinaires et aux mycoses. Leur cicatrisation est plus difficile et leur risque d’infection en cas de blessure (gangrène) est très élevé.
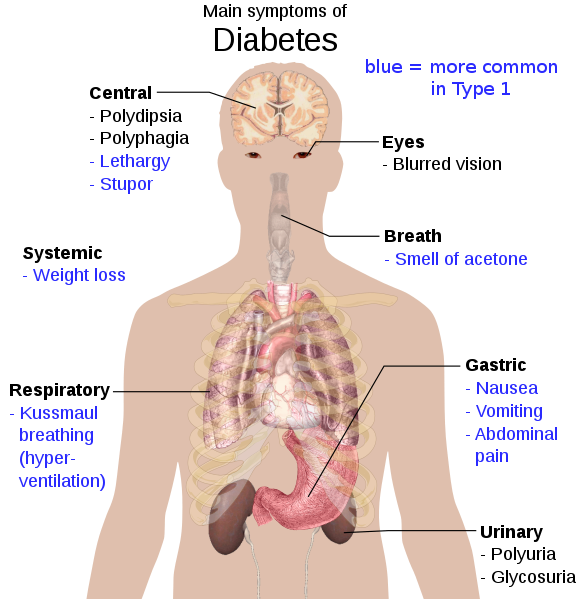
Symptômes du diabète
879px-Main_symptoms_of_diabetes.svg, par Mikael Häggström via Wikimédia Commons, domaine publique, https://commons.wikimedia.org/wiki/File:Main_symptoms_of_diabetes.svg
Il existe 2 catégories de diabète :
le diabète insulino-dépendant ou diabète de type 1
et le diabète insulino-résistant ou diabète de type 2.
Le diabète de type 1
Propriété
Le diabète de type 1 ou DT1 (terme de plus en plus employé dans le milieu médical), appelé aussi diabète insulinodépendant (DID) ou diabète inné (anciennement appelé diabète sucré), apparaît le plus souvent de manière brutale chez l'enfant ou chez le jeune adulte (beaucoup plus rarement chez les personnes plus âgées). Parfois présent depuis la naissance, il peut ne se révéler qu'à l'adolescence.
Dans 90% des cas c’est une maladie auto-immune (présence d'auto-anticorps anti-îlot (ICA) et anti-insuline (IAA)) aboutissant à une destruction des cellules β des îlots de Langerhans et donc à une absence de production d’insuline. De fait, la quasi-totalité des enfants diabétiques n'ont pas d'antécédents familiaux.
Le diabète de type 1 suit une évolution en deux phases, la maladie étant dans un premier temps asymptomatique. Les symptômes ne se manifestent que plusieurs mois voire plusieurs années après le début de la maladie : l'hyperglycémie n’apparaît que lorsque plus de 80 % des cellules bêta des îlots de Langerhans sont détruites.
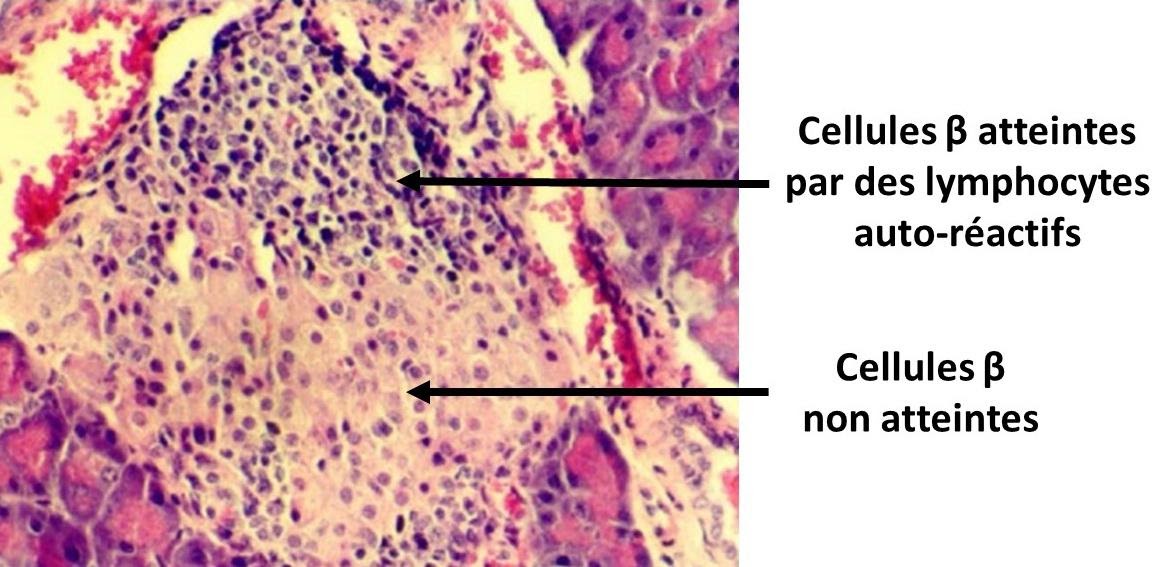
Observation au microscope optique d’un pancréas d’une personne atteinte de DT1
Insulitis_-_Image_from_Journal_of_Autoimmune_Diseases,_2004, par Muhammad T. Tabiin, Christopher P. White, Grant Morahan et Bernard E. Tuch, Hépatocytes exprimant l'insuline non détruits chez les souris transgéniques NOD Dans: Journal of Autoimmune Diseases (Figure 6; lien de l'image originale ), via Wikimédia Commons, CC-BY-2.0, modifié par Sandra Rivière, https://commons.wikimedia.org/wiki/File:Insulitis_-_Image_from_Journal_of_Autoimmune_Diseases,_2004.jpg
Les thérapies actuellement existantes permettent au patient diabétique de mener une vie normale et de réduire fortement les effets néfastes de la maladie.
Le traitement du diabète de type 1 associe régime et prise d'insuline. Le diabétique peut s’alimenter normalement, à condition que cette alimentation soit équilibrée : il doit privilégier les aliments qui ont des indices glycémiques faibles comme les légumes, les fruits non pressés et des préparations à base de céréales complètes.
Les médecins recommandent généralement la pratique d'une activité physique chez le diabétique de type 1 car les muscles consomment du glucose pendant l'activité physique ce qui favorise la baisse de la glycémie.
Le diabétique doit surveiller quotidiennement sa glycémie au bout du doigt en prélevant une goutte de sang et en la déposant sur une bandelette réactive à insérer dans un appareil appelé glucomètre. Cette auto-surveillance est vitale car elle permet au diabétique d'optimiser ses doses d'insuline et de limiter les risques associés à sa maladie.
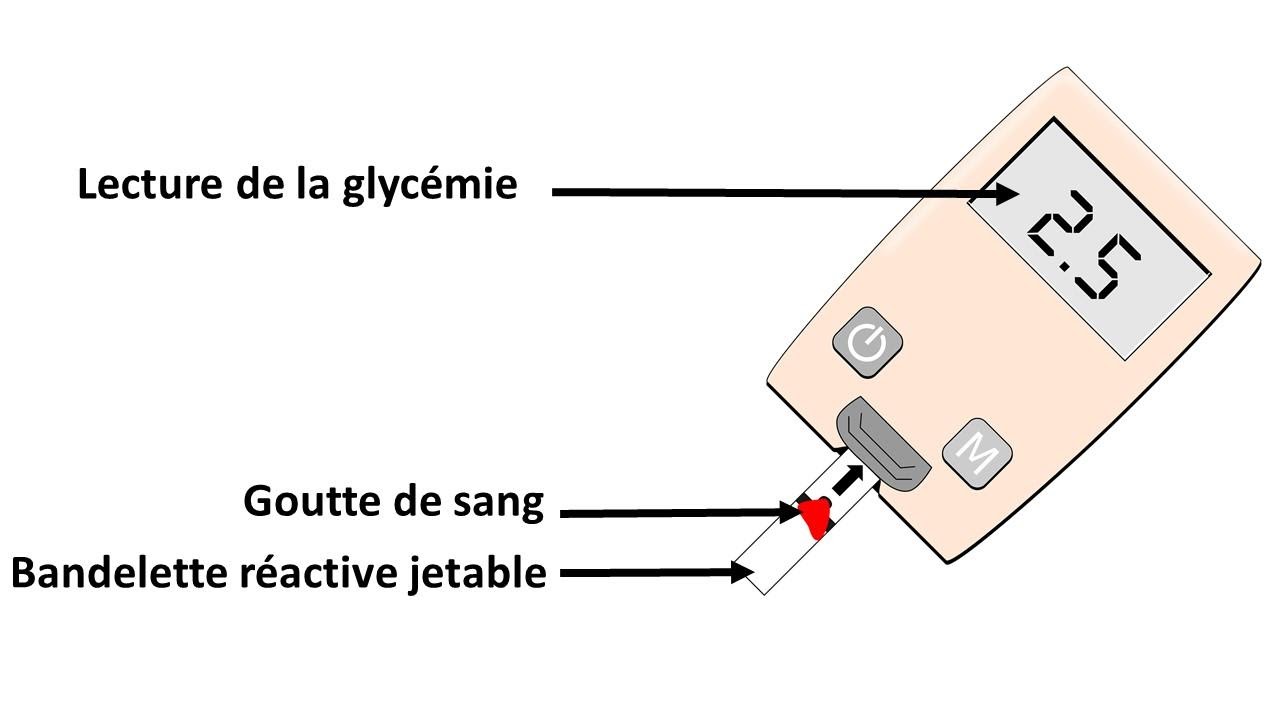
Glucomètre
blood-sugar-2023254_1280, Image par OpenClipart-Vectors de Pixabay, modifié par Sandra Rivière, https://pixabay.com/fr/vectors/sucre-dans-le-sang-diab%C3%A8te-2023254/
Il existe également un capteur de glycémie présentant une petite aiguille transcutanée. Installée pour 14 jours sur le bras, elle permet de surveiller la glycémie de manière plus régulière à l’aide d’un boitier connecté.
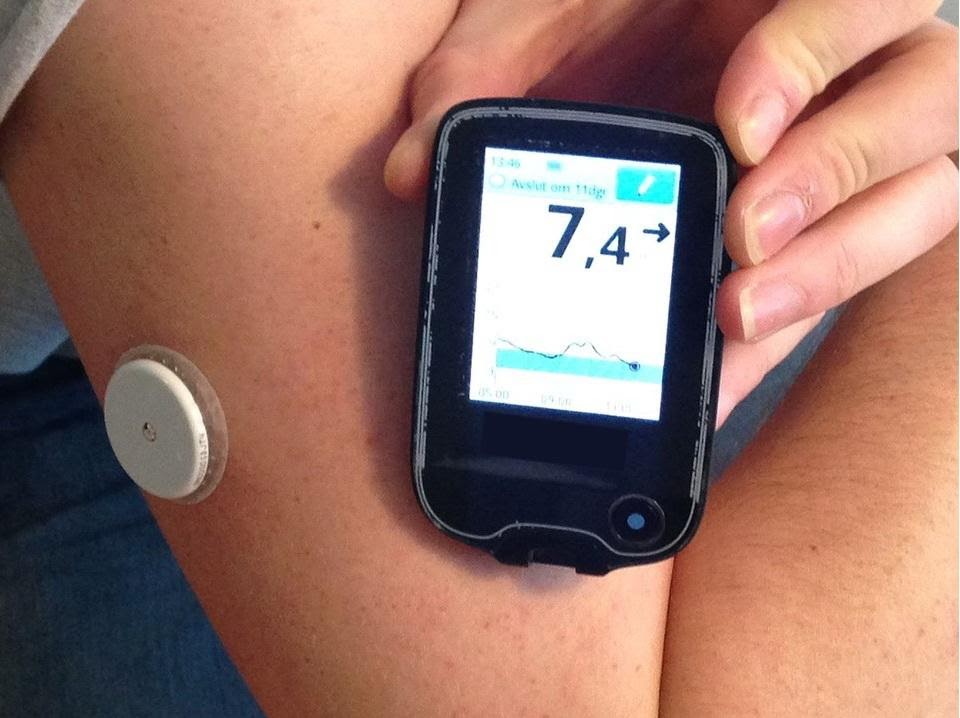
Capteur de glycémie
BGM_twopart, par Sjö, propre travail, via Wikimédia Commons, CC-BY-SA-4.0, modifié par Sandra Rivière
https://commons.wikimedia.org/wiki/File:BGM_twopart.JPG
Remarque
L'insuline ne peut pas être prise par voie orale car elle est détruite par la digestion. Il faut donc l'injecter soit à l’aide d’une aiguille, soit à l’aide d’un stylo injecteur ou encore à l’aide d’une pompe à insuline installée au niveau de l’abdomen.
Insuline injectable
Inzulín, par Mr Hyde sur Wikipedia tchèque, via Wikimédia Commons, domaine publique, https://commons.wikimedia.org/wiki/File:Inzul%C3%ADn.jpg
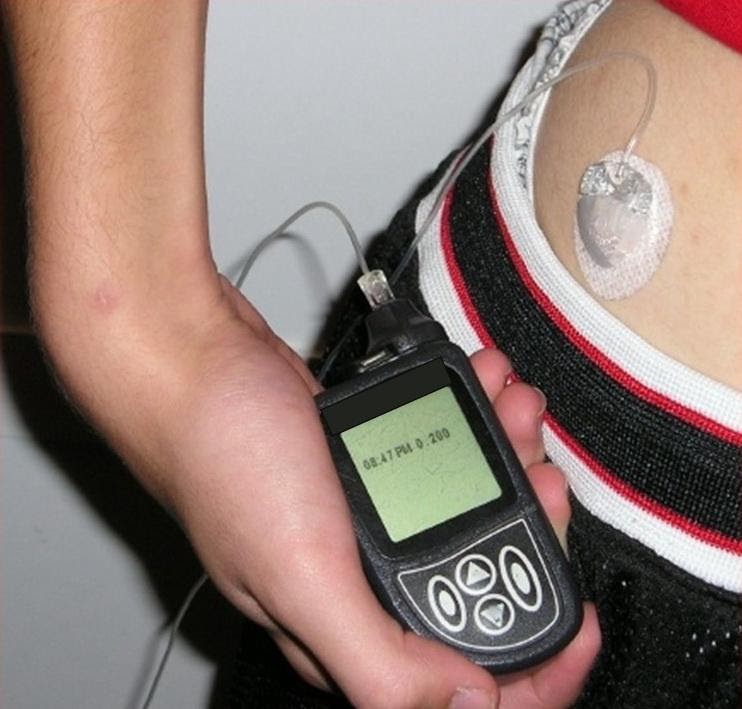
Pompe à insuline
Insulin_pump_with_infusion_set, par Mbbradford sur Wikipedia anglais, via Wikimédia Commons, modifié par Sandra Rivière, domaine publique, https://commons.wikimedia.org/wiki/File:Insulin_pump_with_infusion_set.jpg
Le traitement est à prendre à vie sans interruption. D'autres traitements sont à l'étude, mais actuellement la prise d'insuline est le seul traitement qui permet d'avoir une vie normale sans trop de contraintes. C'est le patient diabétique qui ajuste à chaque repas sa dose d'insuline. Son implication et sa connaissance du traitement sont donc importantes.

Aujourd’hui les médecins tentent des greffes d’îlots de Langerhans. Les îlots récupérés dans au moins 3 pancréas issus de dons post-mortem, sont injectés dans la veine porte du receveur. Le patient devra prendre des médicaments antirejet toute sa vie. Le succès est partiel mais permet de diminuer les doses d’insuline à injecter.
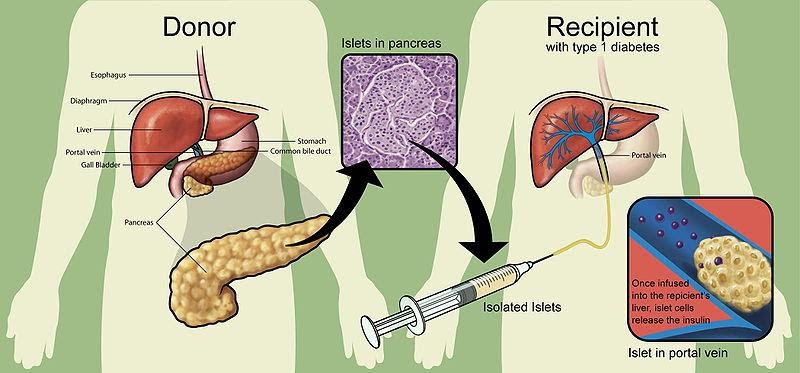
Principe de la greffe d’îlots de Langerhans
1200px-Islet_transplantation_PLoS_Medicine, par Giovanni Maki via Wikimédia Commons, Naftanel MA, Harlan DM (2004) Transplantation d'îlots pancréatiques. PLoS Med 1 (3): e58 ( lien image ), CC-BY-2.5, https://commons.wikimedia.org/wiki/File:Islet_transplantation_PLoS_Medicine.jpg
Le diabète de type 2
Propriété
Le « diabète de type 2 » (DT2) ou « diabète non insulinodépendant » (DNID), aussi appelé « diabète insulino-résistant », « diabète de l'âge mûr », « diabète gras », parfois « diabète acquis », se caractérise par une résistance de l'organisme à l'insuline et par une hyper-insulinémie réactionnelle.
Les cellules effectrices du système réglant présentent une résistance à l’insuline qui augmente avec l’âge et des facteurs environnementaux. Pour compenser cette résistance, le pancréas fabrique davantage d'insuline jusqu'à l'épuisement et la destruction des cellules β des îlots de Langerhans. La sécrétion d’insuline ralentit de plus en plus et la glycémie augmente. Souvent asymptomatique durant des années, la maladie est dépistée par l'examen biologique de la glycémie à jeun ou après stimulation par l'ingestion de sucre (hyperglycémie provoquée orale).
Le diabète de type 2 entraine des complications graves à long terme : infarctus du myocarde, AVC, athérosclérose, insuffisances rénales, maladies hépatiques, atteinte de la rétine, problèmes de cicatrisation…
Ce diabète augmente rapidement dans le monde, y compris chez l'enfant. Dans les pays développés, le diabète est la première cause de cécité chez les 20-65 ans. En 2016, le nombre de malades dépassait largement les premières prédictions de l’OMS faites 15 ans plus tôt, au début des années 2000. En Europe, il y avait, vers 2005, environ 21 millions de diabétiques de type 2 diagnostiqués.
En France, près de 3,5 millions de personnes avaient déclaré cette maladie, auxquels s'ajoutent probablement 600 000 à 700 000 personnes ignorant leur maladie. Aujourd’hui, la prévalence est d’environ 1 français sur 10.
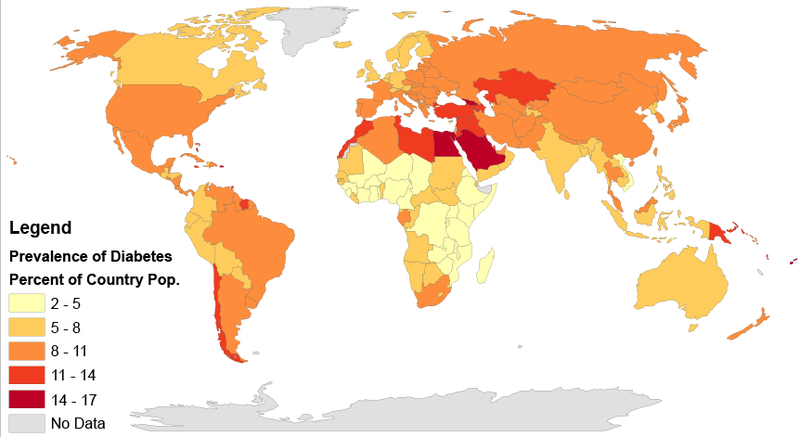
Prévalence mondiale du diabète de type 2 en 2014
Prevalence_of_Diabetes_by_Percent_of_Country_Population_(2014)_Gradient_Map, par Walter Scott Wilkens Université de l'Illinois - Département de géographie et de SIG d'Urbana Champaign, via Wikimédia Commons, CC-BY-SA-4.0, https://commons.wikimedia.org/wiki/File:Prevalence_of_Diabetes_by_Percent_of_Country_Population_(2014)_Gradient_Map.png
Ce diabète est considéré comme une maladie environnementale et émergente, encore mal comprise au début du XXème siècle. La suralimentation et la sédentarité des modes de vie semblent en cause.
La majorité des victimes de diabète de type 2 sont des personnes obèses présentant un fort taux de graisse abdominale. L'obésité chronique induit une résistance accrue à l'insuline pouvant évoluer en diabète. Une perte de poids volontaire ainsi qu’une activité physique réduisent le risque de développer cette maladie.

Mesure du tour de taille par un médecin
obese-3011213_1920, Image par mohamed Hassan de Pixabay, https://pixabay.com/fr/illustrations/ob%C3%A8ses-poids-perte-l-homme-3011213/
Une alimentation trop riche en acides gras saturés favorise le diabète de type 2 alors que les acides gras insaturés d'origine végétale diminuent le risque. Un remplacement des acides gras saturés par des acides gras insaturés chez une personne diabétique améliore la tolérance au glucose et augmente la sensibilité à l'insuline si l'apport total en matières grasses n'est pas excessif (maximum 37 % de l’énergie totale).
Il existe des médicaments antidiabétiques qui aident à contrôler la glycémie en stimulant la production d’insuline ou en retardant l’absorption intestinale des glucides après un repas déclenchant un laps de temps plus long pour permettre à l’organisme de réguler la glycémie.
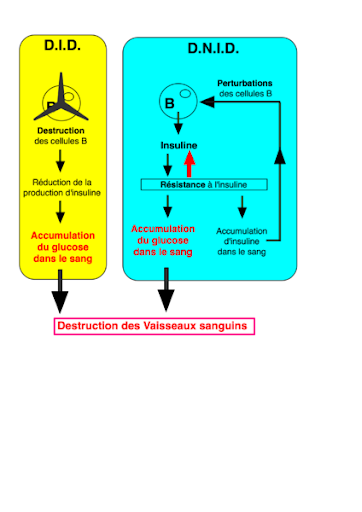
Comparaison des 2 diabètes
Les_diabetes par Pr. Dr Raynal propre travail , via Wikimédia Commons, https://commons.wikimedia.org/wiki/File:Les_diabetes.png
Revenir au chapitre
Commentaires





