


Titrage colorimétrique

Cours
Titrage colorimétrique
Titrage colorimétrique
Sommaire
Dosage
Définition
Un dosage permet de déterminer la quantité de matière ou la concentration d’une espèce chimique dissoute dans une solution.
Un dosage par titrage, ou titrage, est une technique de dosage faisant intervenir une réaction chimique totale et rapide.
Réaction support d'un titrage et dispositif
Propriété
Lors d’un dosage, le réactif titré dont on cherche à déterminer la concentration réagit avec le réactif titrant de concentration connue.
L’équation de réaction support du titrage s’écrit :
Dispositif de titrage
Propriété
Le réactif titré peut être mis dans un bécher ou un erlenmeyer, le réactif titrant est dans une burette.
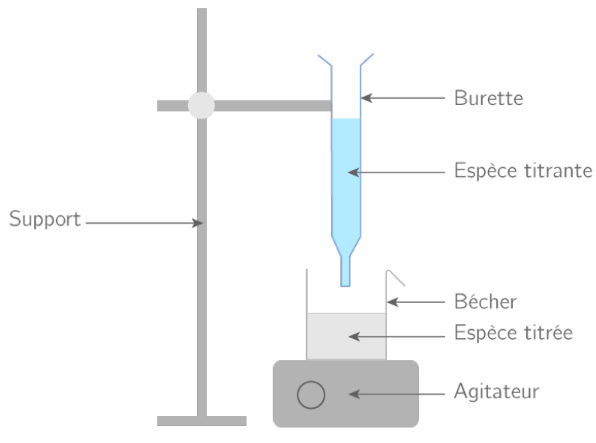
Schéma d'un dosage par titrage
Détermination de la concentration d’un réactif titré
Principe

Au cours du titrage, on verse du réactif titrant jusqu’à ce que le réactif titré ait totalement réagit : l’équivalence est alors atteinte.
Définition
L’équivalence d’un titrage est atteinte lorsqu’on a réalisé un mélange stœchiométrique entre réactif titrant et réactif titré.
Les deux réactifs sont alors consommés.
Avant l’équivalence, le réactif titrant est le réactif limitant car totalement consommé.
Après l’équivalence, c’est le réactif titré qui devient le réactif limitant.
Titrages colorimétriques
Définition
Lors d’un titrage colorimétrique, un changement de couleur du mélange réactionnel permet de repérer l’équivalence :
Une disparition de la teinte (titrage du diiode)
Une apparition de la teinte (titrage du thiosulfate)
Un changement de teinte (titrage du permanganate)
Relation à l'équivalence du titrage
Propriété
À l'équivalence du titrage, on a réalisé un mélange stœchiométrique des réactifs.
Pour une réaction support du titrage :
On a à l'équivalence :
La concentration du réactif titré sera alors :
Revenir au chapitre
Commentaires
Theurel
0
il me semble que "jusqu'à ce qu'elle ait totalement réagi" ne prend pas de t, puisque c'est un participe passé.





