


Les combustions

Cours
Les combustions
Les combustions
Sommaire
Qu'est-ce que la réaction de combustion ?
Définition
La réaction de combustion est une réaction d’oxydo-réduction au cours de laquelle :
Un combustible (ce qui brûle) s’oxyde
Un comburant, généralement le dioxygène, se réduit.
Pour activer une combustion, une énergie doit être apportée.

Le triangle du feu = 3 conditions à réunir pour générer une réaction de combustion : un combustible, un comburant, une énergie d'activation
Energie transférée lors d'une combustion
Définition
Lors de la combustion, le système chimique libère de l’énergie sous forme de chaleur, notée .
Les réactions de combustion étant des réactions exothermiques, elles dégagent de la chaleur et donc .
Propriété
L’énergie transférée lors de la combustion dépend de deux paramètres :
La nature du combustible
La quantité de combustible
Energie molaire de combustion

Pour calculer l’énergie molaire de combustion, on part de l’équation de combustion avec un coefficient de 1 pour le combustible.
Lors d’une réaction de combustion, des liaisons sont rompues (les réactifs) et d’autres sont formées (les produits).
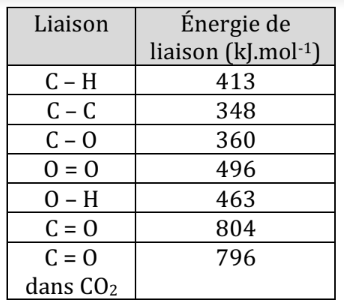
Il suffit donc de connaitre l’énergie de liaison des différentes liaisons des molécules et de faire la différence d’énergie entre celles rompues et celles formées.
Définition
Revenir au chapitre
Commentaires





