


Transformations nucléaires
Les isotopes
Propriété
Comme vu au chapitre 3, un élément chimique est caractérisé par son numéro atomique Z (son nombre de protons).
Il a aussi un symbole qui sera le même quelle que soit sa forme.
L’écriture conventionnelle d’un noyau est avec le symbole de l’élément, le numéro atomique et le nombre de masse (nombre de nucléons).
Définition
Des atomes ou des ions isotopes possèdent le même nombre de protons Z mais pas le même nombre de neutrons et donc de nucléons.
Ainsi, ils ont le même Z mais un A différent.
Les atomes isotopes portent le nom de l’élément chimique suivi du nombre de nucléons.
Exemple
Le Carbone 13 et le Carbone 14 sont des isotopes et s'écrivent : et .
Le Chlore 35 et le Chlore 36 sont des isotopes et s'écrivent : et .
Propriété
Les propriétés chimiques d’un atome sont déterminées par la structure de son cortège électronique.
Des atomes isotopes ont la même réactivité chimique car ils ont le même nombre d’électrons.
Transformation nucléaire
Introduction
Les transformations nucléaires ont lieu constamment. Elles sont spontanées pour la plupart mais certaines peuvent être provoquées.
Définition
Lors d’une transformation nucléaire :
Un ou plusieurs noyaux réactifs se transforment en de nouveau noyaux
Les éléments chimiques ne sont pas conservés
Un rayonnement gamma est émis
Exemple
Un noyau de plutonium 238 se scinde en deux noyaux : un d’uranium 234 et un d’hélium
Propriété
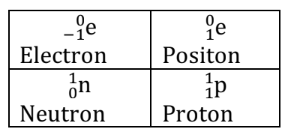
Tout comme les transformations physiques et chimiques, une transformation nucléaire est modélisée par une réaction dans laquelle interviennent les particules qui réagissent et les particules formées.
Une particule est caractérisée par son nombre de masse A et son nombre de charge Z, l’écriture conventionnelle est la même que pour les éléments chimiques.
Propriété
L’équation nucléaire doit rendre compte de la conservation du nombre de masse A et du nombre de charge Z au cours de la transformation.
Exemple
Propriété
Lors d’une transformation nucléaire, une partie de l’énergie nucléaire contenue dans les noyaux réactifs est transformée en énergie rayonnante : le rayonnement gamma .
Dans le Soleil et dans les réacteurs des centrales nucléaires, ce sont des grandes quantités d’énergie qui sont libérées.
Identification de la nature d'une transformation
Propriété
Toutes les transformations (chimique, physique, nucléaire) ont une équation de réaction pour les modéliser.
Pour identifier la nature d’une transformation, il faut analyser les réactifs et les produits.
Le schéma ci-dessous permet d'identifier la nature d'une transformation et de faire la distinction entre réaction chimique, réaction physique et réaction nucléaire :
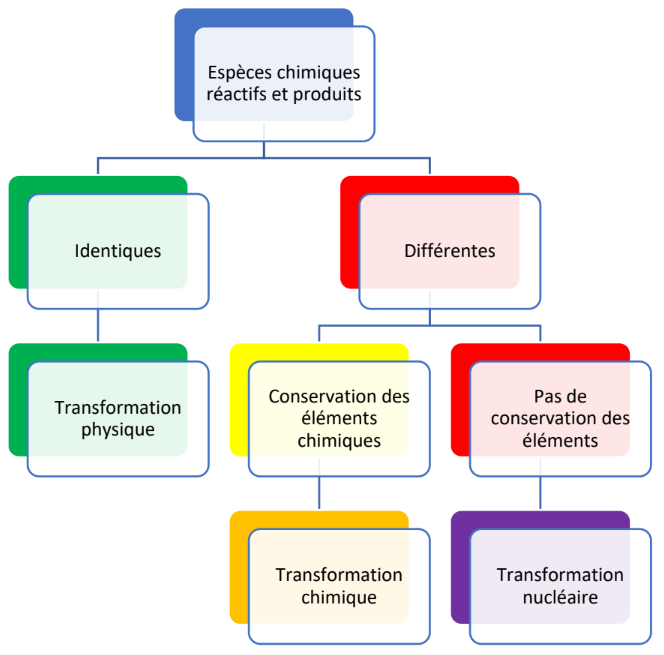
Commentaires
anonyme
1
Déterminer l’écriture conventionnelle des noyaux des atomes de l’élément iode I. Ce n'est pas noté dans le cour.
anonyme
0
je me suis tromper si ya
anonyme
1
J'adore se cour, il est géniale ☺☺☺





